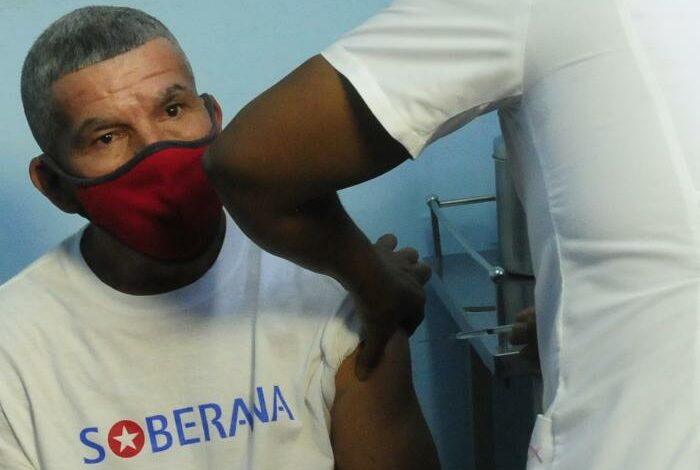
En el periodo que abarcó la etapa inicial de la Fase III se involucraron ocho municipios habaneros, y dentro de estos 31 sitios clínicos y 48 vacunatorios
La primera etapa de la Fase III de los ensayos clínicos del candidato vacunal Soberana 02, que incluyó 44 010 voluntarios y se desarrolló en La Habana hasta el martes, culminó, en apenas 18 días, con resultados alentadores que van confirmando la alta eficacia del antígeno en términos de la seguridad del producto y la respuesta inmune que está generando contra el SARS-CoV-2.
Así lo aseguró la investigadora principal de los ensayos clínicos de Soberana 02, María Eugenia Toledo Román, quien también destacó, durante una comparecencia en la conferencia de prensa del Ministerio de Salud Pública, que el éxito de la etapa inicial se debió, en gran medida, a la disposición de la población para participar en los estudios, lo cual permitió el completamiento de la captación de las personas que van a formar parte del ensayo y la administración de las 44 010 dosis que estaban previstas.
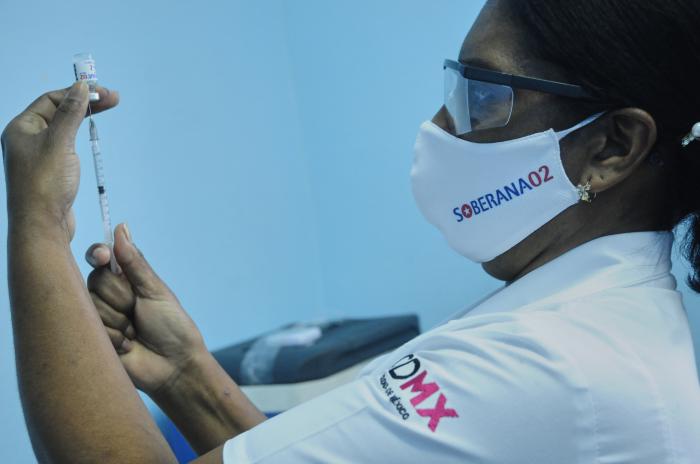
«Hay mucha confianza del pueblo y eso hace que las pérdidas en el estudio sean menores, porque la gente quiere continuar», dijo la especialista, y resaltó que no faltaron voluntarios dispuestos para el ensayo, aun sabiendo que podían ser inyectados con placebo.
Precisó que en el periodo que abarcó la etapa inicial de la Fase III se involucraron ocho municipios capitalinos, y dentro de estos 31 sitios clínicos y 48 vacunatorios.
A propósito de la óptima organización con que contó el proceso, ponderó la investigadora el gran esfuerzo del sistema de Salud para disponer de equipos de investigación preparados, que consiguieran evaluar a los sujetos antes de entrar a la vacunación, consultar cada una de sus enfermedades o preocupaciones, y conseguir el consentimiento firmado de esas personas.
Al referirse a la seguridad del producto demostrada durante la primera etapa, afirmó que más del 82 % de los efectos adversos manifestados por las personas han sido leves, propios de cualquier vacuna, como dolor e inflamación en el sitio de la inyección, fiebre y malestar general.
En tanto, los eventos adversos reportados como graves se deben a sujetos hospitalizados por antígenos positivos al coronavirus. En este caso- explicó la especialista- no se trata de que hayan manifestado complicaciones extremas por el producto, sino que solamente el hecho de la hospitalización se considera peligroso para el paciente y se registra como efecto adverso grave.

Algunas inquietudes sobre el ensayo clínico con Soberana 02
Una de las inquietudes que más genera en la población el ensayo clínico es la aplicación de placebo a una parte de los voluntarios que participan en el proceso.
El doctor en ciencias Rolando Pérez Rodríguez, director de Ciencia e Innovación del Grupo Empresarial BioCubaFarma, explicó, durante la comparecencia del lunes pasado, que un ensayo clínico Fase III, que proporciona la medida de la eficacia de un candidato vacunal, se realiza con un grupo de control previamente seleccionado de acuerdo a determinados criterios de inclusión.
Una parte de esos voluntarios se tratan con el producto de investigación (en este caso el candidato vacunal) y el otro grupo recibe el placebo, un producto que no tiene actividad farmacológica, no es la vacuna y, por tanto, no produce ningún efecto en el organismo.
Sin embargo, el frasco del placebo es idéntico al de la vacuna real, de ahí que los ensayos se realizan a doble ciega, lo que significa que ni el sujeto que es vacunado, ni el que aplica la vacuna, sabe si está aplicando el producto en investigación o el placebo.
Entonces, ¿qué sucede al final del ensayo clínico con los voluntarios que recibieron placebo? ¿Pueden confundir el placebo con el candidato vacunal aquellas personas encargadas de controlar el estudio a ciegas?
María Eugenia Toledo Román aclaró que el estudio va a continuar a ciegas hasta completar el esquema de vacunación de dos y tres dosis del candidato vacunal en unas personas y del placebo en otras, pero, una vez que concluya y se le comunique a cada voluntario el producto que se le inyectó, aquellos que se les aplicó placebo recibirán el esquema de vacunación de mejores resultados en la eficacia.
«Nadie sale del estudio sin haber recibido el esquema de vacunación que está establecido», aseveró.
Acerca de la otra duda planteada por los usuarios, la Investigadora Principal de los Ensayos Clínicos de Soberana 02 aseguró que no hay posibilidad de confusión entre el placebo y antígeno. «Como mismo hay muchas personas trabajando de frente a los voluntarios, hay otras tantas detrás asegurando que esto funcione bien. Ahí está la Empresa Comercializadora de Medicamentos, los trabajadores del IFV asumiendo todo el proceso de codificación, las inspecciones que recibimos de la Agencia Reguladora, el monitoreo conducido por el Centro para el Control de los Ensayos Clínicos (Cencec). Hay muchos mecanismos de aseguramiento que garantizan que se respete el esquema de vacunación asignado a cada sujeto y no se produzcan confusiones con el producto que se le aplica», manifestó.
Asimismo, sobre la posibilidad de que un sujeto participante del estudio dé positivo a la COVID-19, Toledo Román declaró que la persona sí poder resultar contagiada durante el ensayo clínico, porque hay que completar el esquema de vacunación para protegerse realmente contra la enfermedad sintomática. De ahí, la importancia de complementar el efecto de la vacuna con el cuidado y el cumplimiento de las medidas de protección.
A propósito de esta posibilidad, confirmó la investigadora que se han detectado casos con antígenos y PCR positivos al SARS-CoV-2 durante el ensayo clínico. Satisfactoriamente, la mayoría de esos sujetos desarrollaron formas muy leves de la enfermedad, que es otro de los propósitos de los efectos del candidato vacunal.
Una vez que el sujeto da positivo a la pandemia se interrumpe el tratamiento de la vacunación, pues el esquema previsto para los que se infectan es el uso del candidato Soberana Plus.
Por otra parte, al hablar del estudio de intervención controlado que se desarrolla en estos momentos en La Habana, destacó el hecho de que un grupo importante de trabajadores de la Salud y de los centros de la biotecnología, así como personal de riesgo definido por el Minsap, esté administrándose el candidato vacunal voluntariamente y contribuyendo a los análisis de eficacia.
Agregó que estos estudios se van a ir extendiendo paulatinamente a todos los municipios de la capital, con el propósito de realizar una intervención poblacional que proteja finalmente a los habitantes de la ciudad, ante la altísima transmisión del virus que enfrentan.
El estudio de intervención controlado no utiliza placebo y, en este caso, aplica dos dosis de Soberana 02 y una de Soberana Plus en un intervalo 28 días entre cada una.